Mundo Nano | v16n31
http://dx.doi.org/10.22201/ceiich.24485691e.2023.31.69795 | Mundo Nano| julio-diciembre 2023
Artículos de revisión
Ana Saret Ortega-Galindo*
Lucero Díaz-Peralta**
Arturo Galván-Hernández**
Iván Ortega-Blake**
Alejandro Pérez-Riasco***
Yareli Rojas-Aguirre*♦
*Universidad Nacional Autónoma de México, Instituto de Investigaciones en Materiales, Departamento de Polímeros, SupraMatLab. CDMX, México.
**Universidad Nacional Autónoma de México, Instituto de Ciencias Físicas. Cuernavaca, Morelos, México.
***Universidad Nacional Autónoma de México, Instituto de Física, Departamento de Sistemas Complejos. CDMX, México.)
Resumen:
Los liposomas son vesículas artificiales biocompatibles y biodegradables que poseen una estructura con dos compartimentos capaces de albergar moléculas hidrofílicas y lipofílicas, respectivamente. Los liposomas han sido ampliamente investigados durante los últimos veinte años como sistemas de liberación de fármacos, lo cual ha resultado en el desarrollo de diversas tecnologías como liposomas Stealth® y DepoFoam®. Asimismo, han surgido liposomas funcionalizados en su superficie con biomacromoléculas que pueden reconocer blancos biológicos específicos, dando lugar a potenciales terapias de alta selectividad. De igual manera, liposomas que responden a estímulos fisicoquímicos o biológicos y en los que la liberación de un fármaco estaría controlada en función de dicho estímulo. O bien, liposomas que encapsulan 2 o más fármacos, resultando así en terapias de combinación. Los liposomas son las primeras nanomedicinas en alcanzar uso clínico. Actualmente, existen al menos 20 tecnologías liposomales para tratar diversos padecimientos y alrededor de 18 están en fases clínicas de evaluación. La mayoría de liposomas comerciales se utilizan para tratar diferentes tipos de cáncer. Sin embargo, varias formulaciones liposomales para otros padecimientos han mostrado resultados prometedores. En este trabajo revisamos los conceptos básicos sobre liposomas, discutimos los casos de éxito y revisamos aquellas nanoformulaciones que se encuentran en estudios clínicos. Por último, por medio de ciencia de datos, presentamos el panorama actual de la investigación de liposomas en el área de la nanomedicina. Sin duda, los liposomas están y seguirán estando a la vanguardia en el traslado de nanotecnologías en beneficio de la salud de la población.
Palabras clave: liposomas, tecnologías liposomales, >cáncer, targeting, estímulo-sensible, ensayos clínicos.
Abstract:
Liposomes are biocompatible and biodegradable artificial vesicles with a two-compartment structure that can encapsulate both hydrophilic and lipophilic molecules. Liposomes have been extensively studied over the last twenty years, leading to the development of several promising technologies including Stealth® and DepoFoam® liposomes. Also targeted, physicochemical stimuli-responsive, and liposomal-based combined therapies have evolved. Liposomes are the first nanomedicines to reach the clinical use. Currently, up to 20 different liposomal technologies are commercially available, and approximately 18 liposomal formulations are in clinical trials. While most commercial liposomes are used to treat cancer, there are some liposomal developments that have shown promising results for treating other diseases. In this review, we present an overview of the basic concepts of liposomes, breakthroughs in liposomal-based nanoformulations in clinical trials and currently marketed liposomal technologies. Furthermore, using data science tools, we present a comprehensive analysis of current research in liposomes. Undoubtedly, liposomes will continue to be at the forefront of nanotechnologies applied for the benefit of human health.
Keywords: liposomes, liposomal technologies, cancer, targeting, stimuli-responsive, clinical trials.
Fecha de aceptación: 12 Abril 2023
Fecha de publicación: 14 Mayo 2023.
Liposomas: estructura y composición1
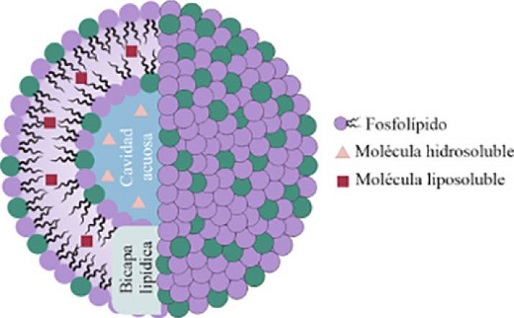
Los liposomas son pequeñas vesículas artificiales conformadas por una bicapa de fosfolípidos que rodean un núcleo acuoso (Figura 1). Estas vesículas varían en tamaño, composición, carga eléctrica y lamelaridad (unilamelares, multilamelares y multivesiculares) (Nsairat, 2022; Sivan, 2018).
Los liposomas pueden encapsular moléculas hidrofílicas en su cavidad acuosa, mientras que en su bicapa lipídica pueden albergar moléculas hidrofóbicas. Estas características estructurales han determinado su enorme relevancia en distintas disciplinas como la biología (dada su similitud con la membrana celular), la medicina, las ciencias farmacéuticas, cosméticas y dermocosméticas (Nakhaei, 2021).
Por su habilidad de encapsular moléculas de diversa naturaleza, los liposomas pueden funcionar como sistemas de liberación de fármacos. En este contexto, los liposomas pueden modificar de manera aparente aspectos como la solubilidad o estabilidad de un fármaco, lo cual favorecerá el comportamiento de dicho fármaco en un ambiente biológico. Además, los liposomas son biocompatibles y biodegradables (Sercombe, 2015).
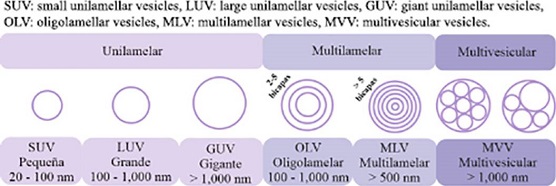
Los liposomas se clasifican en función de su tamaño (que va desde la nanoescala hasta la microescala), y del número de sus bicapas o lamelas (Figura 2) (Liu, 2022).
Los fosfolípidos que forman los liposomas están constituidos por un extremo hidrofílico (cabeza) y un extremo hidrófobo (cola). La cabeza determina la carga superficial del liposoma (neutra, catiónica o aniónica) y generalmente está compuesta de colina, fosfato y glicerol. Por su parte, la cola hidrofóbica está conformada por una o dos cadenas de ácidos grasos de 14 - 18 carbonos (Nsairat, 2022). Los fosfolípidos pueden ser de origen natural (obtenidos de la soya o la yema de huevo) o sintético. Los fosfolípidos más comúnmente usados en la preparación de liposomas se muestran en la Tabla 1 (Van Hoogevest, 2014).
Tabla 1 Fosfolípidos naturales y sintéticos más comunes en la preparación de liposomas.
Fuente: Adaptado de Van-Hoogevest (2014). Además de los fosfolípidos, los liposomas también pueden contener esteroles, siendo
el
colesterol el más común. El colesterol brinda estabilidad física y biológica ya
que
puede modificar la viscosidad o la rigidez de la bicapa a la vez que reduce su
permeabilidad en presencia de fluidos biológicos como la sangre. En ausencia de
colesterol, la bicapa podría sufrir una rotura (Nakhaei, 2021; Kawakami,
2017).
Los liposomas se pueden utilizar para encapsular fármacos hidrofílicos (en el núcleo
acuoso), o hidrofóbicos (en la bicapa). El encapsulamiento protege al fármaco de la
degradación. En caso de que el fármaco sea hidrofóbico, el encapsulamiento podría
ayudar a superar las limitantes fisicoquímicas, biológicas y farmacéuticas asociadas
con su baja solubilidad. Además, los liposomas pueden optimizar los parámetros farmacocinéticos
del fármaco encapsulado, al prolongar su tiempo de vida media, controlar su liberación
en función del tiempo y disminuir su toxicidad (Liu, 2022). Así, el diseño de un liposoma como sistema de liberación de fármacos (SLF) debe
considerar lo siguiente:
El tamaño determinará la biodistribución y la velocidad de eliminación del liposoma.
Si su diámetro es menor a 10 nm se eliminará por vía renal y si es mayor a 200 nm
será retenido mayoritariamente por los hepatocitos, lo cual afectará la distribución
del liposoma (Taléns, 2022).
La temperatura de transición de fase (Tc) es la temperatura a la cual los fosfolípidos cambian de estado físico. Por debajo
de la Tc, los fosfolípidos están ordenados en una fase tipo gel y por encima de ella, se encuentran
en una fase líquida. Los fosfolípidos con una Tc > 37 ºC forman liposomas de una bicapa poco fluida, y, por lo tanto, menos permeables
a temperatura fisiológica. Mientras que fosfolípidos con una Tc < 37 ºC forman liposomas que liberan el fármaco encapsulado en la fase líquida de
forma más rápida (Sharma, 1997). Así, la Tc determinará la fluidez de la bicapa, la liberación del fármaco in vivo y la estabilidad durante el almacenamiento.
Adicionalmente, la Tc se puede modificar con la adición de esteroles (Kawakami, 2017).
Después de su administración, los liposomas que llegan a circulación sistémica pueden
interactuar con las proteínas plasmáticas, lípidos y metabolitos por medio de interacciones
electrostáticas, de Van der Waals e hidrofóbicas, resultando así en la formación de
una corona proteica. A nivel biológico, la corona determina la interacción con células
del sistema inmune; modifica o impide la salida del fármaco del liposoma; o, por el
contrario, deforma la bicapa provocando la fuga del fármaco; limita las interacciones
del liposoma con su blanco terapéutico; e induce efectos inmunogénicos debido a la
pérdida parcial de la estructura secundaria de las proteínas de la corona (Marichal, 2020; Cai, 2019). Dado el impacto de la corona en el desempeño biológico del liposoma, es fundamental
evaluar este aspecto durante los estudios in vitro/in vivo y definir el tipo de recubrimiento que pueda mitigar este fenómeno.
Dada la versatilidad y potencial de los liposomas como sistemas de liberación de fármacos
(SLF), se han desarrollado diversas tecnologías para aumentar su estabilidad coloidal,
hacerlos responsivos a algún estímulo fisicoquímico endógeno o exógeno; o bien, para
dirigirlos a un blanco biológico específico.
Son liposomas simples (Figura 3a), los cuales, después de
su administración, suelen ser eliminados rápidamente de circulación sistémica
al ser
fagocitados por los macrófagos del sistema retículo endotelial (RES) (Sercombe, 2015).
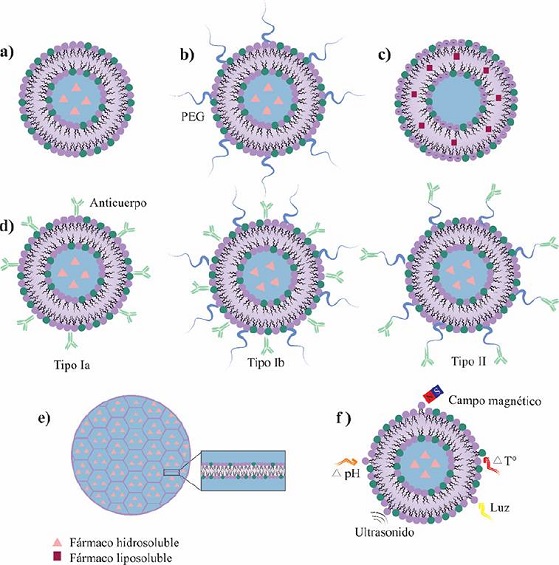
Figura 3. Esquema de liposoma: a) convencional; b) Stealth®; c) iónico; d) inmunoliposoma; e)
DepoFoam®, y, f) estímulo-sensible. Fuente: Elaboración de los autores. Los liposomas Stealth® (sigilosos) tienen polietilenglicol (PEG) enlazado covalentemente
a las cabezas polares de los fosfolípidos (Figura 3b). También se conocen como liposomas pegilados. La pegilación de la superficie del
liposoma mejora su estabilidad coloidal. Reduce la interacción con proteínas plasmáticas
y lipoproteínas. Además, lo hace invisible frente a RES, y, por lo tanto, optimiza
la farmacocinética al prolongar el tiempo de vida media del fármaco en circulación
sistémica (Čeh, 1997; Nsairat, 2022).
Los fosfolípidos más comunes en esta tecnología son: DSPE, DPPE y DOPE. El peso molecular
del PEG suele ser de 2000 Da (Nosova, 2019).
La carga de la superficie del liposoma puede ser positiva o negativa y se puede modular
dependiendo del fosfolípido a utilizar. La carga superficial del liposoma genera un
campo eléctrico que incrementa el espesor de la bicapa lipídica pudiendo así aumentar
la cantidad de fármaco liposoluble encapsulado (Figura 3c).
Son liposomas con anticuerpos monoclonales (mAb) o fragmentos de anticuerpos (Fab
o scFv) acoplados a su superficie (NCI 2019). Pueden ser liposomas convencionales (tipo Ia), pegilados (tipo Ib) y (tipo II)
pegilados con anticuerpos acoplados en los extremos distales de las cadenas de PEG
(Figura 3d). El objetivo del inmunoliposoma es dirigirse a un blanco terapéutico, de manera
específica, por medio de la unión del liposoma a su receptor en la célula blanco.
También se puede favorecer la internalización celular mediada por receptores de superficie
y promover la acumulación del fármaco dentro de la célula, lo cual es altamente deseable
si se trata de quimioterapéuticos (Kontermann, 2011).
Esta tecnología encapsula fármacos en una plataforma liposomal de tipo MVV. Estas
estructuras se componen de un panal de numerosas cámaras acuosas de diferente tamaño,
delimitadas por una única bicapa lipídica que, físicamente, se asemejan a burbujas
de jabón (Figura 3e). Esta tecnología puede proporcionar mayor estabilidad, encapsular fármacos de forma
más eficiente y asegurar una liberación sostenida de fármacos en comparación con los
liposomas unilamelares (Angst, 2006).
Son liposomas que incorporan materiales que responden a estímulos físicos (térmico,
óptico, magnético) o químicos (pH, redox, enzimas) para promover o desencadenar la
liberación de fármaco en respuesta a dichos estímulos y controlar así la liberación
de un fármaco de manera temporal. Así, los liposomas funcionalizados con biomoléculas
en su superficie para reconocer y dirigirse al blanco terapéutico, y que además incorporan
materiales estímulosensibles, han resultado sumamente atractivos como potenciales
terapias contra el cáncer (Figura 3f) (Lee, 2017).
Los liposomas son las primeras nanomedicinas aprobadas para uso clínico utilizadas
con éxito desde hace dos décadas (Tabla 2) como terapias antifúngicas, antinflamatorias, anticancerígenas e, incluso, terapias
génicas (Bulbake, 2017).
Tabla 2 Tecnologías liposomales en uso clínico..
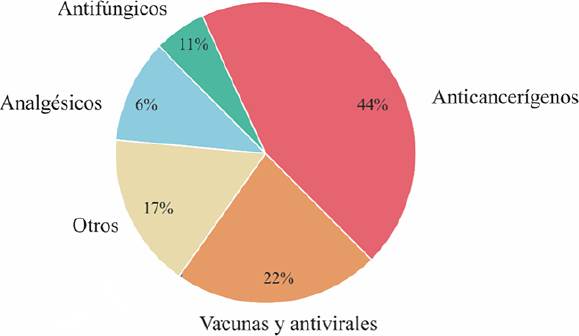
Fuente: Adaptado de Taléns (2022), Liu (2022), Beltrán (2019), Bulbake (2017), EMA (2015). Hemos representado gráficamente la información de la Tabla 2 para facilitar la identificación de las áreas de aplicación de los liposomas siendo
evidente el predominio de las quimioterapias (Figura 4).
Figura 4. Áreas terapéuticas con tecnologías liposomales aprobadas clínicamente. Otros (sistema
nervioso, ocular y respiratorio). Fuente: Elaboración de los autores. El cáncer está entre los primeros cinco lugares de causas de mortalidad en México
y a nivel mundial (INEGI, 2022; WHO, 2022). Se sabe que el cáncer se desarrolla por una proliferación celular descontrolada
activada por vías de señalización y falta de apoptosis (muerte celular). Inicia en
un sitio localizado, pero tiende a propagarse a diferentes partes del cuerpo (metástasis).
En el cáncer, el microambiente del tejido donde se desarrolla el tumor suele ser anormal.
Hay ausencia de vasos linfáticos funcionales e hipoxia. El pH es más ácido que en
el resto del cuerpo y hay sobrexpresión de algunas enzimas. Además, se forman vasos
sanguíneos inmaduros, discontinuos y fenestrados de manera rápida y descontrolada,
lo cual se conoce como efecto de permeabilidad y retención aumentada (EPR, por sus
siglas en inglés) (Taléns, 2022). Las fenestraciones rondan entre 10-800 nm. Por lo tanto, si se tienen liposomas
en ese rango de tamaño, se favorecerá su acumulación en el tejido tumoral (acumulación
pasiva) (Hu, 2022), al mismo tiempo que son retenidos debido a la deficiencia del sistema linfático.
Se considera que liposomas entre 100 y 200 nm se acumulan preferentemente en el tejido
tumoral por el efecto EPR (Taléns, 2022).
Como las células tumorales sobrexpresan algunos receptores de membrana que promueven
su crecimiento desenfrenado, la superficie de los nanoliposomas se puede funcionalizar
con ligandos que reconozcan dichos receptores para dar paso a lo que se conoce como
acumulación activa (selectiva o targeted) que, además, podría estar favorecida por la acumulación pasiva, mediada por el tamaño
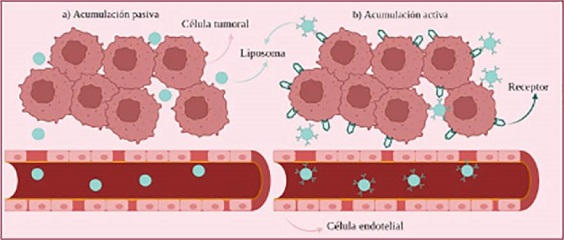
nanométrico del liposoma (Figura 5) (Mahato, 2017).
Figura 5. Representación de la acumulación: a) pasiva, y, b) activa. Fuente: Elaboración de los autores. Por lo tanto, liposomas en los que por su tamaño se favorezca la acumulación pasiva,
con superficies funcionalizadas para que reconozcan una célula o tejido en particular
y en los que se controle la liberación del fármaco por medio de un estímulo físico
o químico (liposomas inteligentes) son las nanoplataformas de liberación de fármacos
que más expectativas han generado en el desarrollo de terapias novedosas contra el
cáncer.
Los liposomas son las primeras nanomedicinas aprobadas para terapias contra el cáncer.
De un total de 20 formulaciones liposomales aprobadas para uso clínico (Tabla 2), 9 están indicadas para dicho padecimiento. De estas 9 formulaciones, 5 de ellas
(Doxil®, Myocet®, Zolsketil®, DaunoXome® y Vyxeos™) contienen doxorrubicina o daunorrubicina,
que son derivados de antraciclinas. Las antraciclinas son fármacos muy eficaces como
quimioterapéuticos, pero con uso limitado debido a su cardiotoxicidad y una resistencia
espontánea o adquirida al tratamiento (Aubel, 1984). A continuación, describimos las tecnologías liposomales utilizadas en terapias
contra el cáncer.
Doxil® fue la primera formulación liposomal aprobada para el tratamiento de algunos
tipos de cáncer. Consiste en liposomas Stealth®, tipo SUV, de 100 nm de diámetro,
compuestos de HSPC, MPEG2000-DSPE y colesterol. Encapsula doxorrubicina en la cavidad
acuosa. Se utiliza para el tratamiento del cáncer de ovario avanzado y sarcoma de
Kaposi asociado con el VIH. Los comienzos de Doxil® datan de la década de los años
sesenta del siglo XX, con varios intentos fallidos, y que actualmente han sido un
pilar fundamental en el desarrollo de tecnologías liposomales, hoy en día exitosos
(Tabla 3). El artículo Doxil® - The first FDA-approved nano-drug: Lessons learned es una excelente revisión sobre la historia del desarrollo de Doxil® (Barenholz, 2012).
Tabla 3 Requisitos y soluciones de la formulación liposomal de Doxil®.
Doxil® resultó más eficaz que la doxorrubicina libre, logró mejorar el perfil toxicológico
de la doxorrubicina y mejoró sus características farmacocinéticas debido a su tamaño,
pegilación y estabilidad de bicapa (Gabizon, 1994).
Son liposomas MLVs de 190 nm de diámetro, compuestos de EPC y colesterol. Encapsulan
doxorrubicina y emplean la técnica de carga remota, con eficiencias de encapsulamiento
del 99%. Se utiliza en combinación con ciclofosfamida como tratamiento de primera
línea en pacientes con cáncer de mama. La lógica detrás de su diseño es similar a
Doxil® (con el objetivo de mejorar el perfil de seguridad de la doxorrubicina y mantener
su eficacia antitumoral) sin embargo, Myocet® es un sistema liposomal no pegilado
por lo cual, libera más del 90% del fármaco durante las primeras 24 horas posteriores
a su administración (Doxil® libera menos del 10 % de su doxorrubicina en el mismo
periodo de tiempo). En ausencia de PEG, los liposomas son visibles ante RES pero al
mismo tiempo se reduce la prevalencia de un efecto secundario que parece estar ligado
a liposomas Stealth®, conocido como eritrodisestesia palmar-plantar (Waterhouse, 2001).
Son liposomas SUVs no pegilados de 45-80 nm de diámetro, compuestos de DSPC y colesterol
con daunorrubicina en la cavidad acuosa que se utiliza para el tratamiento del sarcoma
de Kaposi asociado al VIH.
DaunoXome ha mostrado tasas de respuesta superiores al 50%. Además, mejora el perfil
farmacocinético de daunorrubicina; aumenta su permanencia en circulación sistémica
con una liberación sostenida de alrededor de 36 horas. Asimismo, ha mostrado una reducción
considerable en la cardiotoxicidad del fármaco (Forssen, 1997).
Son liposomas LUVs de 110 nm de diámetro, compuestos de DSPC, DSPG y colesterol. Son
los primeros liposomas aprobados en terapia dual encapsulando dos fármacos en su cavidad
acuosa: citarabina y daunorrubicina. Se utiliza para el tratamiento de leucemia mieloide
aguda causada por quimioterapias previas y para mielodisplasias de diagnóstico reciente.
Las ventajas de Vyxeos se basan en la sinergia antitumoral mejorada de sus fármacos,
en la reducción de la frecuencia de dosis administradas en comparación con los tratamientos
tradicionales, y en el aumento de la tasa de supervivencia de los pacientes (EMA, 2022).
Son liposomas Stealth®, tipo SUV, de 100 nm de diámetro, conteniendo doxorrubicina,
compuestos de HSPC, MPEG2000-DSPE y colesterol. Zolsketil demostró ser bioequivalente
a Doxil® y está indicado para pacientes con cáncer de mama, mieloma múltiple (en combinación
con bortezomib) y sarcoma de Kaposi. De igual manera, los liposomas de Zolsketil pueden
permanecer por largo tiempo en circulación sanguínea sin ser detectados por RES y
se ha demostrado su acumulación selectiva en comparación con doxorrubicina libre (EMA, 2022).
Es el primer sistema DepoFoam™ en alcanzar un uso clínico. Son liposomas MVVs de 20,000
nm de diámetro, compuestos de DOPC, DPPG, trioleína y colesterol conteniendo citarabina
en las cavidades acuosas, lo cual permite su liberación sostenida durante 14 días.
Este sistema logró una dosificación menos frecuente. Demostró prolongar el tiempo
de supervivencia y una mejor calidad de vida de los pacientes respecto a aquellos
tratados con citarabina libre (Angst, 2006). En 2017, DepoCyt™ se retiró del mercado debido a problemas de producción a largo
plazo no revelados (McDonald, 2017)
Son liposomas MLVs de 2,000-3,500 nm, compuestos de POPC y DOPS. Contienen el principio
activo mifamurtida (muramil tripéptido fosfatidiletanolamina, MTP-PE). MTP-PE es un
derivado lipofílico fabricado del dipéptido muramilo, componente de las paredes celulares
bacterianas. Mepact® tiene como objetivo reducir el desarrollo y recurrencia de las
metástasis al usar el MTP-PE como un ligando específico del receptor NOD2 que se encuentra
en monocitos y en macrófagos.
Fue la primera inmunoterapia aprobada para el tratamiento de tumores óseos no metastásicos
resecables de alto grado en niños, adolescentes y adultos jóvenes, posterior a una
resección quirúrgica macroscópica completa. El uso de Mepact® ha demostrado prolongar
la supervivencia de los pacientes sin que reaparezca la enfermedad y redujo el riesgo
de muerte (EMA 2013).
Son liposomas LUVs de 130-150 nm de diámetro, se componen de SM y colesterol. Contienen
sulfato de vincristina en la cavidad acuosa y se usan para tratar leucemia linfoblástica
aguda cuando los pacientes no han respondido a terapias antileucémicas anteriores.
Marqibo®, con un 95% de vincristina encapsulada, demostró aumentar el tiempo en circulación
sistémica del fármaco, a pesar de no estar pegilado. Asimismo, su seguridad y eficacia
fueron aceptables (Silverman, 2013). Marqibo® fue aprobado en 2012, bajo las regulaciones de aprobación acelerada de
la FDA, a reserva de verificar su beneficio clínico en la etapa de post-comercialización,
lo cual no se logró concretar debido a la dificultad de reclutamiento de pacientes,
por lo que fue retirado en 2022 (FDA, 2022).
Son liposomas Stealth® MLVs de 110 nm de diámetro, compuestos por HSPC, MPEG-DSPE
y colesterol. Está indicado para el tratamiento de adenocarcinoma de páncreas metastásico
que no respondió al tratamiento con gemcitabina. Se prepara con un gradiente de polialquilamida
de alto pKa para facilitar la encapsulación de irinotecán. Así, Onivyde™ logra el
90% de encapsulación del fármaco, el cual se libera de manera prolongada. Onivyde™
se utiliza en combinación con leucovorina y fluorouracilo (Bulbake, 2017).
Los liposomas son los nanosistemas que mejor han enfrentado los desafíos de los estudios
clínicos, en comparación con el resto de nanomateriales estudiados como posibles SLF.
Los ensayos clínicos son aquellos que se llevan a cabo en humanos para poner a prueba
la eficacia de los fármacos y se dividen en 4 fases. En la fase I se administra la
formulación a un grupo reducido de pacientes (5-15) a dosis bajas para conocer el
potencial de la formulación frente a un padecimiento específico. En las fases II y
III se incrementa el número de pacientes (25-100 y varios cientos, respectivamente),
y la dosis administrada se aproxima a la ideal. En la fase IV, el número de pacientes
aumenta a unos miles. En esta fase se estudia la seguridad del tratamiento a través
del tiempo (American Cancer Society, 2020).
Son varios los sistemas liposomales que actualmente se encuentran en las fases clínicas
I-III (Figura 6).
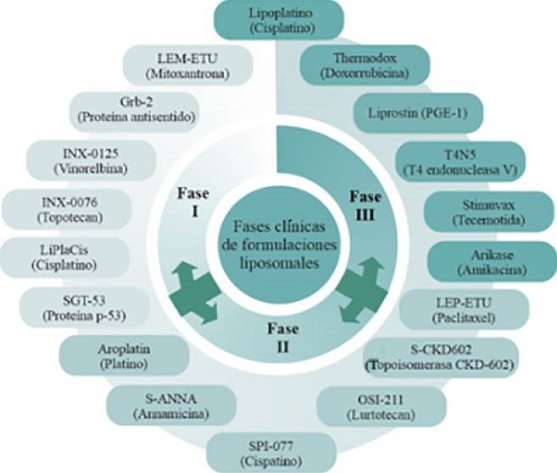
Figura 6. Diagrama de formulaciones liposomales fases clínicas I-III. Las flechas indican que
hay flujo dinámico entre las fases. Fuente: Modificado de Bulbake (2017). Todos los liposomas en fases I y II contienen fármacos anticancerígenos, mientras
que los ensayos de fase III incluyen, además de anticancerígenos, otros activos. A
continuación, se describen brevemente los sistemas liposomales en fase III.
Son liposomas GUVs de 200-300 nm de diámetro, compuestos de DPPC y colesterol, conteniendo
el fármaco amikacina. Su uso se contempla para tratar infecciones bacterianas al ser
administrado por inhalación para liberar el fármaco de manera prolongada en los pulmones.
Es la primera tecnología liposomal de administración pulmonar que ha llegado a evaluación
clínica (Bulbake, 2017).
Es una vacuna liposomal tipo MLV, compuesta por DMPG, DPPC y colesterol. Se diseñó
para tratar cánceres que expresan el antígeno mucina 1 asociado con tumores, como
el carcinoma de pulmón de células no pequeñas. Desafortunadamente, en 2013 se suspendieron
sus ensayos al no aumentar la supervivencia general de los pacientes (Kroemer, 2013).
Es una loción liposomal MLV, compuesta por PC, PE, ácido oleico y hemisuccinato de
colesterol (CHEMS). El sistema liposomal encapsula la endonucleasa V del bacteriófago
T4, enzima de reparación del ADN. Se diseñó para tratar cáncer de piel y xeroderma
pigmentoso (enfermedad genética caracterizada por una piel extremadamente sensible
a la luz ultravioleta). T4N5 se administra por vía tópica para penetrar en las células
dérmicas (Yarosh, 2001).
Son liposomas MLVs conteniendo prostaglandina E-1 (PGE-1), un vasodilatador, inhibidor
plaquetario, agente antinflamatorio y antitrombótico. Liprostin™ está dirigido a enfermedades
vasculares, como reestenosis posterior a la angioplastia. La reestenosis se asocia
con el bloqueo de los vasos sanguíneos en el corazón y las piernas luego de un cateterismo
(Bulbake, 2017; Liprostin Group, 2020).
Son liposomas LUVs de 110 nm de diámetro, compuestos de DPPG, SPC, MPEG-DSPE y colesterol.
Contiene cisplatino y se encuentra en fase I para derrame pleural maligno; en fase
II para cáncer de mama y cáncer gástrico. Asimismo, en fase II/III para cáncer de
páncreas y ensayos de fase III para cáncer de pulmón de células no pequeñas (Fantini, 2011).
Son liposomas Stealth® termosensibles compuestos por DPPC, MSPC, DSPEPEG-2000 conteniendo
doxorrubicina. En este caso, la liberación del fármaco será después de un ligero aumento
de temperatura. ThermoDox® es el primer y único sistema termosensible que ha alcanzado
las fases clínicas. Está dirigido a cáncer primario de hígado (carcinoma hepatocelular)
y a cáncer de mama recurrente de la pared torácica. Se administra por vía intravenosa
y el aumento de temperatura ocurre de manera localizada por medio de ablación por
radiofrecuencia para generar hipertermia moderada (39.5-42 °C). El aumento de la temperatura
modifica la permeabilidad de la bicapa, facilitando la liberación de doxorrubicina
(Dou, 2017). ThermoDox® es un sistema muy novedoso cuyos resultados de pruebas in vivo fueron
prometedores. Entró a fases clínicas de evaluación y los ensayos clínicos avanzaron
rápidamente hasta que, en 2013, ya en fase III, se detuvieron, debido a la falta de
evidencia sobre su eficacia (Liu, 2022).
El hecho de que Stimuvax® y ThermoDox® hayan fracasado en la fase III nos da una lección
importante: los liposomas son sistemas prometedores pero impredecibles, reflejando
así la necesidad de investigar a detalle la relación entre su tamaño, composición
e interacción con las interfaces biológicas.
Para tener un panorama general sobre la investigación que ha predominado en cuanto
al diseño y desarrollo de tecnologías liposomales, analizamos un conjunto de 4,340
publicaciones sobre liposomas como SLF, utilizando herramientas de la ciencia de datos.
Para ello, se utilizó la base de datos Scopus, de la cual se obtuvieron las investigaciones
publicadas entre 1975-2022, obtenidas bajo los siguientes criterios de búsqueda:
Palabras clave: se seleccionaron artículos que tuvieran las palabras liposome, drug y delivery haciendo uso del código booleano AND: liposome AND drug AND delivery.
Tipo de documento: se seleccionaron únicamente artículos de investigación (excluyendo
revisiones, capítulos de libro, memorias de congresos, comentarios, etcétera).
Idioma: se incluyeron solamente los artículos publicados en idioma inglés. De esta manera se obtuvo un conjunto de 4,340 artículos, cuyos abstracts se descargaron para su posterior análisis, el cual se llevó a cabo siguiendo la
metodología previamente desarrollada dentro de nuestro grupo de investigación, basado
en ciencia de redes para detección de comunidades (Figura 7) (Rincón, 2021). El propósito de la minería de texto fue caracterizar el universo de 4,340 documentos
e identificar patrones que nos permitieran mostrar el panorama de la investigación
en este campo. La describimos brevemente a continuación.
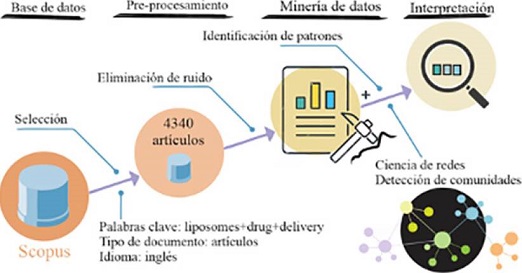
Figura 7. Proceso de la minería de texto en artículos científicos sobre liposomas como sistemas
de liberación de fármacos. Fuente: Modificado de Bulbake (2017) Pre-procesamiento: se realizó empleando la librería Natural Language ToolKit (NLTK) de Python 3.0 (McKinney, 2010). Esta etapa consistió en eliminar aquellas palabras “ruido” que pudieran interferir
con el análisis; todas las palabras se transformaron a minúsculas; se removieron todos
los símbolos de puntuación; y se eliminaron aquellas palabras que no aportan gran
significado a las oraciones, como a, the, an, on, this, is, for, large, numerous, used, without, entre otras.
Minería: los datos pre-procesados se analizaron a través del mayor componente conectado
(LCC), que detecta las conexiones dentro del conjunto de datos para así formar una
red. Posteriormente, se aplicó el algoritmo de Louvain para detectar las comunidades
dentro de la red con mayor densidad, es decir, grupos de artículos con contenido semántico
similar. El análisis se llevó a cabo utilizando diversas herramientas de librerías
en Python.
Interpretación: la detección de comunidades nos permitió conocer la frecuencia relativa
de las palabras en cada una de dichas comunidades. Así, analizando las 3 palabras
más frecuentes en cada comunidad, logramos identificar patrones dentro del universo
de documentos.
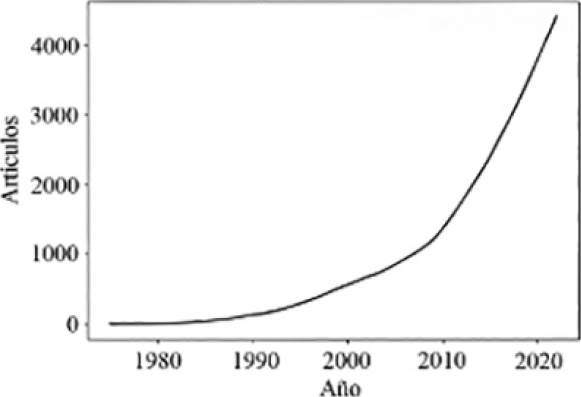
La Figura 8 muestra la suma acumulada de publicaciones de liposomas como SLF desde 1975 hasta
2022. Se observa que a mediados de los años 90, el interés por estas estructuras comenzó
a emerger, y a partir del año 2000 hay un crecimiento acelerado en su investigación
que se mantiene hasta la actualidad. De hecho, de 1975 a 1999 hay solamente 515 publicaciones,
mientras que de 2000 a 2022, hay 3,825 artículos. Lo anterior refleja el punto de
inflexión generado a partir de la aprobación clínica de doxorrubicina liposomal (Doxil®)
y del inicio de los ensayos clínicos de ThermoDox®, dos parteaguas en la historia
de liposomas como SLF.
Figura 8. Suma acumulada de publicaciones de liposomas como SLF, 1975-2022. Fuente: Elaboración de los autores. Debido a que la mayoría de artículos se han publicado después del año 2000, el análisis
de detección de comunidades se realizó solamente para el conjunto de 3,825 artículos.
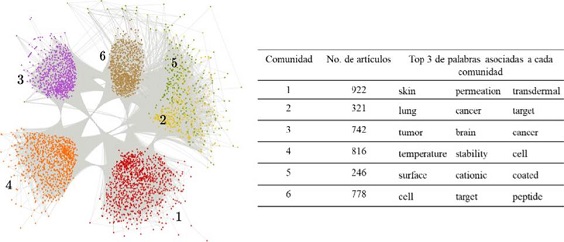
Los resultados muestran que los artículos se agruparon en 6 comunidades. La red de
comunidades, el tamaño de cada comunidad (la cantidad de artículos en cada una de
ellas), así como las 3 palabras más frecuentes asociadas a cada grupo se muestran
en la Figura 9.
Figura . Representación gráfica de la red formada por las publicaciones de liposomas como SLF
del 2000-2022, así como las palabras representativas de cada comunidad. Fuente: Elaboración de los autores. Resulta muy interesante que la comunidad 1 es la más grande y hace referencia a liposomas
como sistemas de liberación tópica y transdérmica. Dentro de las estrategias utilizadas
para promover la penetración de fármacos a través de la piel, se encuentran las nano
y micro vesículas, de las cuales los liposomas han jugado un rol importante. Aunque
los liposomas convencio nales no logran llegar a las capas más profundas de la piel,
es posible que por medio de la modulación de la flexibilidad de la bicapa lipídica,
su lamelaridad, tamaño y la carga superficial, se dé lugar a sistemas con una eficiencia
similar a la de una inyección subcutánea. Así, liposomas ultradeformables menores
a 150 nm son capaces de penetrar la piel y liberar el fármaco en sus capas profundas.
Los liposomas catiónicos flexibles pueden acumularse, por medio de interacciones electrostáticas,
en los folículos capilares, desde donde pueden difundir más fácilmente. Los fosfolípidos
de la piel, que se encuentran cargados negativamente, pueden interactuar con los liposomas
catiónicos, favoreciendo su penetración hasta capas profundas de la piel. Cabe destacar
que los liposomas también se han considerado como potenciales modelos de membranas
para estudiar la permeación en piel (El Maghraby, 2008).
Después del cáncer de mama, el cáncer de pulmón es el más común a nivel mundial, y
en 2020 el que causó más muertes (WHO, 2022). Con la finalidad de mejorar las estrategias terapéuticas, se ha explorado ampliamente
el uso de SLF, en particular, los liposomas, que han sido los más estudiados para
tal fin. De hecho, son alrededor de 12 formulaciones liposomales las que se encuentran
en ensayos clínicos, incluyendo aquellas que contienen doxorrubicina, cisplatino,
paclitaxel, irinotecan y lurtotecan. Destaca el caso de la combinación de cisplatino
liposomal en combinación con paclitaxel, así como el de la vacuna liposomal conteniendo
tecemotida, que han demostrado ocasionar menos efectos adversos y tener resultados
prometedores (Canão, 2022; Wang, 2020). La comunidad 2 resalta la importancia de los lipomas para este padecimiento.
La comunidad 3 agrupó los artículos en función de las palabras tumor, cerebro y cáncer. De todas las nanomedicinas, los liposomas han sido los más investigados para tratar
los tumores cancerosos que se desarrollan en el cerebro. Si bien los liposomas convencionales
no pueden atravesar la barrera hematoencefálica (BHE) asociada con tumores cerebrales,
la modificación de la superficie de los liposomas con algunos ligandos (anticuerpos,
péptidos, aptámeros, entre otros) para atravesar dichas barreras, ha mostrado resultados
alentadores (Mojarad, 2021). Incluso, ya hay algunos prototipos de liposomas funcionalizados en ensayos clínicos
fase I para malignidades cerebrales. Por ejemplo, 2B3-101 (G-technology™), un liposoma
pegilado de ~95 nm, cargado con doxorrubicina, funcionalizado con glutatión en estado
reducido (GSH), para que entregue su carga en el cerebro vía transportadores de GSH
sin alterar la integridad de la BHE. Por otro lado, está 2B3-101, que ha llegado a
fases clínicas I/IIa para pacientes con glioma recurrente y cáncer de mama con metástasis
en cerebro. Otro caso es C225-ILs-Dox, un inmunoliposoma Stealth® conteniendo doxorrubicina.
Esta nanovesícula está modificada en sus superficies por fragmentos Fab de cetuximab
y está en estudios clínicos de fase I para gliomas. MM-398 es un liposoma convencional
de ~110 nm conteniendo irinotecan que se encuentra en fase clínica I para glioma.
Se ha postulado que el carácter altamente lipofílico de MM-398 le permite atravesar
la BHE (Mojarad, 2021; Shaw, 2022).
Lo anterior evidencia la importancia de la modificación de las propiedades de superficie
de los liposomas, las cuales determinan su comportamiento biológico y su efectividad
como SLF. Más allá de introducir cargas positivas o negativas a la superficie del
liposoma, la incorporación de moléculas para orientación activa (anticuerpos, péptidos,
aptámeros, azúcares, proteínas) sigue siendo un área de investigación con grandes
expectativas. Los liposomas también pueden estar recubiertos con materiales poliméricos
para aumentar su estabilidad coloidal, evitar el reconocimiento por RES, favorecer
su farmacocinética e impartir algunas otras propiedades biológicas. Además de PEG,
los recubrimientos más comunes son: quitosano, polisacáridos, poli-L-lisina, ácido
hialurónico y polielectrolitos (Dymec, 2022; Noble, 2014; Torchilin, 2008; Keith, 2022; Kristensen, 2014; Dass, 2006). Los liposomas pueden estar recubiertos por materiales sensibles a algún estímulo
físico o químico que detone la liberación del fármaco (Lee, 2017), que junto con los liposomas biomiméticos (recubiertos por membranas celulares)
están comenzando a cobrar enorme interés (Pratygyan, 2020). La importancia de las características de la superficie de los liposomas se ve reflejada
en las comunidades 5 y 6.
Por último, la comunidad 4 indica que 816 artículos se agruparon en función de la
palabra temperatura. Esta palabra puede estar relacionada con aspectos de estabilidad coloidal e integridad
del liposoma a diferentes temperaturas, las cuales dependen de la Tc de los fosfolípidos que constituyen la vesícula. Si se conocen bien las Tc, se puede modular la permeabilidad de la bicapa y por lo tanto controlar la liberación
del fármaco. Bajo esta premisa, Needham y colaboradores diseñaron en el año 2000 un liposoma con doxorrubicina cuya liberación rápida era desencadenada por un aumento
moderado en la temperatura (~42 ºC). Esta formulación la conocemos actualmente como
ThermoDox® (Ver Sección ThermoDox®), que, a partir de la eficacia mostrada en estudios
preclínicos, se trasladó rápidamente a ensayos clínicos en 2006. A pesar de que los
ensayos clínicos se detuvieron en 2013, ThermoDox® ha sido un parteaguas en el diseño
de liposomas termosensibles, reflejado en un continuo incremento en el número de publicaciones
desde 2006 (Dou, 2017).
Si bien la temperatura ha sido el estímulo físico más explorado para controlar la
liberación de fármacos contenidos en liposomas, también se ha investigado ampliamente
el control de la liberación por medio de luz (UV e infrarrojo cercano), campos magnéticos
y ultrasonido (Lee 2017; Ashrafizadeh 2022). Asimismo, la liberación mediada por cambios en el pH, en presencia de algunas enzimas
o en respuesta a los procesos de óxido-reducción extra e intracelular. Así, en las
últimas dos décadas, los liposomas pasaron de ser simples vesículas anfifílicas, a
nanosistemas “inteligentes” (estímulo-sensibles) con gran potencial de éxito.
La ciencias de los materiales junto con la nanotecnología han permitido el diseño
y estudio de formulaciones liposomales inteligentes y multifuncionales. Por ejemplo,
liposomas que mejoren las técnicas de diagnóstico introducien do agentes de contraste
para resonancia magnética nuclear (gadoteridol) y tomografía computarizada (iohexol).
O bien, agentes que permitan rastrear al liposoma. Si estas vesículas llevan además
una carga de fármaco, se tendrá una plataforma que entregue el fármaco y haga diagnóstico
de manera simultánea (es decir, un teranóstico) (Aryasomayajula, 2017).
A pesar de tener las bases y la intención de desarrollar sistemas exitosos, los liposomas
son impredecibles y los desafíos por superar no son pocos. Por ejemplo, su inestabilidad
fisicoquímica originada por procesos de oxidación e hidrólisis pueden provocar efectos
secundarios no deseados y reducir su eficacia. Su inestabilidad coloidal en medios
fisiológicos, formación de la corona de proteínas e interacciones con el sistema inmune
pueden provocar fallas en la liberación del fármaco (Nakhaei, 2021). Por ello, a pesar de las ventajas que podrían ofrecer los liposomas responsivos
a estímulos y las grandes expectativas que generan, en particular en terapias contra
el cáncer, existen todavía numerosos retos que deben ser cuidadosamente abordados
para su adecuado progreso a la clínica. La eficacia observada en modelos in vitro/in vivo deberá correlacionarse con aquella observada en estudios clínicos. La toxicidad de
estos liposomas inteligentes también se debe estudiar a detalle. Por ello, la investigación
en liposomas convencionales sigue siendo de enorme relevancia, pues, aunque no se
consideren “inteligentes”, son y seguirán siendo una fuente de generación de valioso
conocimiento para el diseño y desarrollo racional de nuevos liposomas, para cáncer
y otros padecimientos; así como para el entendimiento de las barreras biológicas a
las que se enfrentan las nanomedicinas. En otras palabras, para que las tecnologías
liposomales en uso clínico sean cada vez más frecuentes y beneficien la salud de la
población.
Las propiedades únicas de los liposomas los han convertido en los nanosistemas más
utilizados para la entrega de una amplia gama de agentes terapéuticos y de diagnóstico
con diferentes propiedades fisicoquímicas. Su composición puede modificarse fácilmente
para brindar propiedades específicas a la bicapa lipídica. De esta manera, se puede
prolongar el tiempo en circulación sistémica del fármaco y superar limitantes asociadas
con dicho fármaco como inestabilidad e insolubilidad acuosa. Al ser de escala nanométrica,
se puede promover su acumulación en algunos tejidos tumorales por el efecto EPR. Cuando
están funcionalizados en su superficie con ligandos de reconocimiento, se puede favorecer
su acumulación únicamente en el tejido tumoral, reduciendo así los efectos adversos
de los quimioterapéuticos que encapsulan. Los liposomas son las primeras nanomedicinas
que han alcanzado el uso clínico y han cobrado particular relevancia en terapias contra
el cáncer. Además, las tecnologías liposomales comienzan a destacar como nanomedicinas
para tratar otros padecimientos. Los liposomas han demostrado una gran capacidad para
superar algunas limitaciones de las terapias convencionales y, sin duda, en los años
por venir serán las nanomedicinas las que seguirán estando a la cabeza en su traslado
a la clínica.
Fosfatidilcolina (PC) Fosfatidiletanolamina (PE) Fosfatidilcolina de soya (SPC) Fosfatidilcolina de soya hidrogenada (HSPC) Diestearoilfosfatidilcolina (DSPC) Fosfatidilcolina de huevo (EPC) 1-palmitoil-2-oleoil-fosfatidilcolina (POPC) Dipalmitoilfosfatidilcolina (DPPC) Dioleoilfosfatidilcolina (DOPC) Diestearoilfosfatidilglicerol (DSPG) Dipalmitoilfosfatidilglicerol (DPPG) Dioleoilfosfatidilserina (DOPS) Dipalmitoilfosfatidiletanolamina (DPPE) Esfingomielina (SM) Miristoilestearoil fosfatidilcolina (MSPC) Dimiristoilfosfatidilglicerol (DMPG) N-(carbamil-metoxipolietilenglicol 2000)-1,2-diestearoil-sn-glicero-3-fosfoetanolamina
(MPEG2000-DSPE)
Food and Drug Administration (FDA) European Medicines Agency (EMA), Tecnología liposomal (Tec. Lip.) Año de aprobación (año) Administración (Adm.) Intramuscular (IM) Intravenosa (IV) Intratecal (IT) Inhalación (INH) Fármaco descontinuado (*) Enhanced Permeability and Retention Effect (EPR).
ACS (American Cancer Society) . (2020). Types and phases of clinical trials. https://www.cancer.org/.
Angst, M. S. y Drover, D. R. (2006). Farmacología de medicamentos formulados con DepoFoam™.
Clin Pharmacokinet, 45: 1153-1176. https://doi.org/10.2165/00003088200645120-00002.
Aryasomayajula, B., Salzano, G. y Torchilin, V. P. (2017). Multifunctional liposomes.
Methods in molecular biology, 1530: 41-61, Clifton, N. J. https://doi.org/10.1007/978-14939-6646-2_3.
Ashrafizadeh, M., Delfi, M., Zarrabi, A., Bigham, A., Sharifi, E., Rabiee, N., PaivaSantos,
A. C., Kumar, A. P., Tan, S. C., Hushmandi, K., Ren, J., Zare, E. N. y Makvandi, P.
(2022). Stimuli-responsive liposomal nanoformulations in cancer therapy: Pre-clinical
& clinical approaches. Journal of Controlled Release: Official Journal of the Controlled Release Society, 351: 50-80. https://doi.org/10.1016/j.jconrel.2022.08.001.
Aubel-Sadron, G. y Londos-Gagliardi, D. (1984). Daunorubicin and doxorubicin, anthracycline
antibiotics, a physicochemical and biological review. Biochimie, 66(5): 333-52. https://doi.org/10.1016/0300-9084(84)90018-x.
Barenholz, Y. (2012). Doxil®-the first FDA-approved nano-drug: lessons learned. Journal of Controlled Release: Official Journal of the Controlled Release Society , 160(2), 117-134. https://doi.org/10.1016/j.jconrel.2012.03.020.
Beltrán, E., López, A., Higuera, I., Velázquez, J. y Cardona A. (2019). Nanomedicine
review: clinical developments in liposomal applications. Cancer Nano, 10: 11. https://doi.org/10.1186/s12645-019-0055-y.
Bulbake, U., Doppalapudi, S., Kommineni, N. y Khan, W. (2017). Liposomal formulations
in clinical use: an updated review. Pharmaceutics, 9(2): v12. https://doi.org/10.3390/pharmaceutics9020012.
Cai, R. y Chen, C. (2019). The crown and the scepter: Roles of the protein corona
in nanomedicine. Advanced Materials, 31(45): e1805740. https://doi.org/10.1002/adma.201805740.
Canão, F., Ferreira, H., Neves, N. M., (2022), Liposomal formulations for lung cancer
treatment in the last two decades: a systematic review. Journal of Cancer Research and Clinical Oncology, 148(9): 2375-2386. https://doi.org/10.1007/s00432-022-04079-x.
Čeh, B., Winterhalter, M., Frederik, P. M., Vallner, J. J. y Lasic, D. D. (1997).
Stealth® liposomes: from theory to product. Advanced Drug Delivery Reviews, 24(2-3): 165-177. https://doi.org/10.1016/S0169-409X(96)00456-5.
Dass, C. R. y Choong, P. F. (2006). Selective gene delivery for cancer therapy using
cationic liposomes: in vivo proof of applicability. Journal of Controlled Release: Official Journal of the Controlled Release Society , 113(2): 155-163. https://doi. org/10.1016/j.jconrel.2006.04.009.
Dou, Y., Hynynen, K. y Allen, C. (2017). To heat or not to heat: challenges with clinical
translation of thermosensitive liposomes. Journal of Controlled Release: Official Journal of the Controlled Release Society , 249: 63-73. https://doi.org/10.1016/j.jconrel.2017.01.025.
Dymek, Michał y Sikora, Elżbieta. (2022). Liposomes as biocompatible and smart delivery
systems - The current state. Advances in Colloid and Interface Science, 309: 102757. https://doi.org/10.1016/j.cis.2022.102757.
El Maghraby, G. M., Barry, B. W. y Williams, A. C. (2008). Liposomes and skin: from
drug delivery to model membranes. European Journal of Pharmaceutical Sciences: Official Journal of the European Federation
for Pharmaceutical Sciences, 34(45): 203-222. https://doi.org/10.1016/j.ejps.2008.05.002.
EMA (European Medicines Agency). (2013). European public assessment report summary for the public, Mepact, mifamurtide. https://www.ema.eu.
EMA (European Medicines Agency). (2015). Mosquirix: Opinion on medicine for use outside EU. https://www.ema.eu.
EMA (European Medicines Agency). (2022). An overview of Zolsketil pegylated liposomal and why it is authorised in the EU. Zolsketil
pegylated liposomal (doxorubicin). https://www.ema.eu.
Fantini, M., Gianni, L., Santelmo C., Drudi F., Castellani C., Affatato A., Nicolini
M., Ravaioli, A., (2011). Lipoplatin treatment in lung and breast cancer. Chemotherapy Research Practice, 2011: 125192. https://doi.org/10.1155/2011/125192.
FDA (Food and Drug Administration) . (2022). Withdrawal of approval of new drug application for MARQIBO. Federal Register, FDA-2022-N-0354, 89, 84, 2564425645.
Forssen, E. (1997). The design and development of DaunoXome® for solid tumor targeting
in vivo. Advanced Drug Delivery Reviews , 24(2-3): 133-150. https://doi.org/10.1016/S0169-409X(96)00453-X.
Gabizon, A., Isacson, R., Libson, E., Kaufman, B., Uziely, B., Catane, R., Ben-Dor,
C. G., Rabello, E., Cass, Y. y Peretz, T. (1994). Clinical studies of liposome-encapsulated
doxorubicin. Acta oncologica, 33(7): 779-786, Stockholm, Suecia. https://doi.org/10.3109/02841869409083948.
Hu, M. y Huang, L. (2022). Strategies targeting tumor immune and stromal microenvironment
and their clinical relevance. Advanced Drug Delivery Reviews , 183: 114137. https://doi.org/10.1016/j.addr.2022.114137.
INEGI (Instituto Nacional de Estadística y Geografía) . (2022). Estadísticas de defunciones registradas en el año 2021, 83-90. https://www.inegi.org.
Kawakami, Lisa M., Yoon, Bo Kyeong, Jackman, Joshua A., Wolfgang, Knoll, Weiss, Paul
S. y Cho, Nam-Joon. (2017). Understanding how sterols regulate membrane remodeling
in supported lipid bilayers. Langmuir, 33(51): 14756-14765. https://doi.org/10.1021/acs.langmuir.7b03236.
Keith L. Willes, Sydney A. McFarland, Trent E. Johnson, Daniel R. Hart y Walter F.
Paxton. (2022). Modulating and modeling the surface ζ potential of hybrid lipid/polymer
nanovesicles: implications for surface modification and drug delivery. ACS Applied Nano Materials, 5(10): 13820-13828. https://doi.org/10.1021/acsanm.2c01407.
Kontermann, R. E. (2011). Inmunoliposomas. En Schwab, M. (ed.), Encyclopedia of cancer. Berlín, Heidelberg: Springer. https://doi.org/10.1007/978-3-642-164835_2997.
Kristensen, Kasper, Urquhart, Andrew J., Thormann, Esben y Andresen, Thomas L. (2016).
Binding of human serum albumin to PEGylated liposomes: insights into binding numbers
and dynamics by fluorescence correlation spectroscopy. Nanoscale, 8(47): 19726-19736, The Royal Society of Chemistry. http://dx.doi.org/10.1039/C6NR05455B.
Kroemer, G., Zitvogel, L., Galluzzi, L., (2013). Victories and deceptions in tumor
immunology: Stimuvax®. Oncoimmunology, 2(1): e23687. https://doi.org/10.4161/onci.23687.
Lee, Y. y Thompson, D. H. (2017). Stimuli-responsive liposomes for drug delivery.
Wiley interdisciplinary reviews. Nanomedicine and Nanobiotechnology, 9(5). https://doi.org/10.1002/wnan.1450.
Liprostin Groupk. (2020). Vascular pulmonary diseases. http://www.LiprostinGroup.com.
Liu, P., Chen, G., Zhang, J. (2022). A review of liposomes as a drug delivery system:
Current status of approved products, regulatory environments, and future perspectives.
Molecules, 27(4): 1372. https://doi.org/10.3390/molecules27041372.
Mahato, Rubi. (2017). Emerging nanotechnologies for diagnostics, drug delivery, and medical devices. Chapter
2 -Multifunctional micro- and nanoparticles, micro and nano technologies. Elsevier, 21-43. http://dx.doi.org/10.1016/B978-0-32342978-8.00002-4.
Marichal, L., Degrouard, J., Gatin, A., Raffray, N., Aude, J., Boulard, Y., Pin, S.
(2020). From protein corona to colloidal self-assembly: The importance of protein
size in protein-nanoparticle interactions. Langmuir, 36(28): 8218-8230. https://doi.org/10.1021/acs.langmuir.0c01334.
McDonald, G. (2017). Pacira to stop making DepoCyt due to long-term production problems. https://www.outsourcing-pharma.com.
McKinney, W. (2010). Data structures for statistical computing in Python. Proceedings of the 9th Python in Science Conference, 56-61, https://doi.org/10.25080/Majora-92bf1922-00a.
Mojarad-Jabali, S., Farshbaf, M., Walker, P. R., Hemmati, S., Fatahi, Y., Zakeri-Milani,
P., Sarfraz, M. y Valizadeh, H. (2021). An update on actively targeted liposomes in
advanced drug delivery to glioma. International Journal of Pharmaceutics, 602: 120645. https://doi.org/10.1016/j.ijpharm.2021.120645.
Nakhaei, P., Margiana, R., Bokov, D. O., Abdelbasset, W. K., Jadidi, Kouhbanani, M.
A., Varma, R. S., Marofi, F., Jarahian, M. y Beheshtkhoo, N. (2021). Liposomes: structure,
biomedical applications, and stability parameters with emphasis on cholesterol. Front. Bioeng. Biotechnol, 9: 705886. https://doi.org/10.3389/fbioe.2021.705886.
NCI(National Cancer Institute) . (2019). Immunotherapy to treat cancer. National Institutes of Health. https://www.cancer.gov/about-cancer/treatment/types/immunotherapy.
Needham, D., Anyarambhatla, G., Kong, G. y Dewhirst, M. W. (2000). A new temperature-sensitive
liposome for use with mild hyperthermia: characterization and testing in a human tumor
xenograft model. Cancer Research, 60(5): 1197-1201. www.scopus.com.
Noble, G. T., Stefanick, J. F., Ashley, J. D., Kiziltepe, T. y Bilgicer, B. (2014).
Ligandtargeted liposome design: challenges and fundamental considerations. Trends in Biotechnology, 32(1): 32-45. https://doi.org/10.1016/j.tibtech.2013.09.007.
Nosova, A. S., Koloskova, O. O., Nikonova, A. A., Simonova, V. A., Smirnov, V. V.,
Kudlay, D., Khaitov, M. R. (2019). Diversity of PEGylation methods of liposomes and
their influence on RNA delivery. Medchemcomm, 10(3): 369-377. https://doi.org/10.1039%2Fc8md00515j.
Nsairat, H., Khater, D., Sayed, U., Odeh, F., Al Bawab, A., Alshaer, W. (2022) Liposomes:
structure, composition, types, and clinical applications. Heliyon, 8(5): e09394. https://doi.org/10.1016%2Fj.heliyon.2022.e09394.
Pratigyan Dash, Anna Maria Piras, Mamoni Dash. (2020). Cell membrane coated nanocarriers
- An efficient biomimetic platform for targeted therapy. Journal of Controlled Release, 327: 546-570. ISSN 0168-3659. https://doi.org/10.1016/j.jconrel.2020.09.012.
Rincón-López, J., Almanza-Arjona, Y. C., Riascos, A. P., Rojas-Aguirre, Y. (2021).
When cyclodextrins met data science: unveiling their pharmaceutical applications through
network science and text-mining. Pharmaceutic, 13(8): 1297. https://doi.org/10.3390/pharmaceutics13081297.
Rojas-Aguirre, Y., Aguado-Castrejón, K., González-Méndez, I. (2016). La nanomedicina
y los sistemas de liberación de fármacos: ¿la (r)evolución de la terapia contra el
cáncer? Educación Química, 27(4): 286-291. https://doi.org/10.1016/j.eq.2016.07.002.
538">
Sercombe, L., Veerati, T., Moheimani, F., Wu, S. Y., Sood, A. K., Hua, S. (2015).
Advances and challenges of liposome assisted drug delivery. Front. Pharmacol., 6: 286. https://doi.org/10.3389/fphar.2015.00286.
Sharma, Amarnath y Sharma, Uma S. (1997). Liposomes in drug delivery: Progress and
limitations. International Journal of Pharmaceutics , 154(2): 123-140, 03785173. https://doi.org/10.1016/S0378-5173(97)00135-X.
Shaw, T. K. y Paul, P. (2022). Recent approaches and success of liposome-based nano
drug carriers for the treatment of brain tumor. Current Drug Delivery, 19(8): 815-829. https://doi.org/10.2174/1567201818666211213102308.
Silverman, J. A., Deitcher, S. R. (2013). Marqibo® (vincristine sulfate liposome injection)
improves the pharmacokinetics and pharmacodynamics of vincristine. Cancer Chemother Pharmacol, 71(3): 555-64. https://doi.org/10.1007/s00280012-2042-4.
Sivan-Peretz D., Dima-Shamrakov, Maxim-Varenik, Erez-Koren, Einat-Nativ-R., Yechezkel-Barenholz,
Oren-Regev. (2018). Practical aspects in size and morphology characterization of drug-loaded
nano-liposomes. International Journal of Pharmaceutics , 547(1-2): 648-655. ISSN 0378-5173. https://doi.org/10.1016/j.ijpharm.2018.06.037.
Taléns-Visconti, R., Díez-Sales, O., De Julián-Ortiz, J. V. y Nácher, A. (2022). Nanoliposomes
in cancer therapy: marketed products and current clinical trials. International Journal of Molecular Sciences, 23(8): 4249. https://doi.org/10.3390/ijms23084249.
Torchilin-Vladimir, P. (1996). How do polymers prolong circulation time of liposomes?
Journal of Liposome Research, 6(1): 99-116. https://doi.org/10.3109/08982109609037204.
Van-Hoogevest, P. y Wendel, A. (2014). The use of natural and synthetic phospholipids
as pharmaceutical excipients. European Journal of Lipid Science and Technology, 116(9): 1088-1107. https://doi.org/10.1002/ejlt.201400219.
Wang, Wei y Hao, Yuhao y Liu, Yusheng y Li, Rui y Huang, Da‐Bing y Pan, Yue‐Yin. (2020).
Nanomedicine in lung cancer: Current states of overcoming drug resistance and improving
cancer immunotherapy. Wiley Interdisciplinary Reviews. Nanomedicine and Nanobiotechnology , 13(1). https://doi.org/10.1002/wnan.1654.
Waterhouse, D. N., Tardi, P. G., Mayer, L. D. y Bally, M. B. (2001). A comparison
of liposomal formulations of doxorubicin with drug administered in free form: changing
toxicity profiles. Drug Safety, 24(12): 903-920. https://doi.org/10.2165/00002018-200124120-00004.
WHO (World Health Organization) . (2022). Cancer. https://www.who.int/news.
Yarosh, Daniel B. (2001). Enhancement of repair of UV damage in humans. Comprehensive Series in Photosciences, 3(31): 593-612. Elsevier. https://doi.org/10.1016/S1568-461X(01)80066-1. 1Las abreviaturas utilizadas a lo largo de este artículo, se encuentran al final del mismo, antes de las referencias.
◊Los autores agradecen al Consejo Nacional de Ciencia y Tecnología (Conacyt) (beca
Conacyt de maestría con No. CVU: 1146548); al Programa de Apoyo a Proyectos de Investigación
e Innovación Tecnológica (DGAPA-PAPIIT, UNAM): PAPIIT-IA200821 y PAPIIT-100920; y
al Proyecto Conacyt-Fordecyt-Pronaces-74884.
Liposomas como sistemas de liberación de fármacos
Tamaño
Temperatura de transición de fase
Interacciones con proteínas plasmáticas
Tecnologías liposomales
Liposomas convencionales
Liposomas Stealth®
Liposomas iónicos (catiónicos o aniónicos)
Inmunoliposomas
DepoFoam®
Liposomas estímulo-sensibles
Tecnologías liposomales en uso clínico
Liposomas en cáncer
Tecnologías liposomales como terapias contra el cáncer
Doxil®
Myocet®
Daunoxome
Vyxeos
Zolsketil
DepoCyt™ * Aprobación retirada en 2017
Mepact®
Marqibo® * Aprobación retirada en 2022
Onivyde™
Liposomas en estudios clínicos
Arikace™
Stimuvax®
T4N5
Liprostin™
Lipoplatino™
ThermoDox®
La investigación en liposomas
Resultados
Tendencias en investigación
Conclusiones
Abreviaturas:
Referencias
Notas